全球首款!赛诺菲每周1次血友病A疗法获FDA批准上市
- 2023-02-24 18:00:19 健康一线
- 健康
2月23日,赛诺菲宣布,FDA已批准A型血友病治疗药物efanesoctocog alfa的生物制品许可申请(BLA),这是一种first-in-class高持续性的凝血因子VIII替代疗法。FDA曾授予Efanesoctocog alfa突破性疗法认定、快速通道资格以及孤儿药资格。
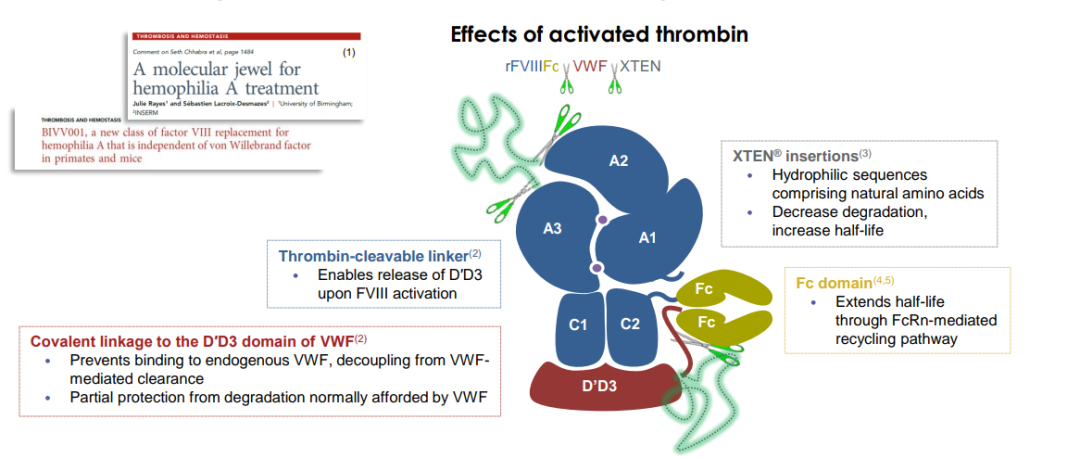
Efanesoctocog alfa(商品名:ALTUVIIIO)是一款新型的凝血因子VIII疗法,通过将凝血因子VIII与Fc、血管性血友病因子(vWF)部分区域和XTEN多肽片段融合在一起,克服vWF对FVIII半衰期延长限制,显著延长药品在血液循环内的时间。该疗法旨在通过每周1次的预防性给药,维持正常的FVIII活性水平以延长对A型血友病患者的出血保护。
 此次上市申请是基于一项开放标签、多中心的III期研究(XTEND-1)数据。该研究纳入了159例12岁及以上患者,旨在评估每周1次接受efanesoctocog alfa对既往接受过凝血因子VIII(FVIII)替代疗法的严重A型血友病患者的安全性、有效性和药代动力学特征。
此次上市申请是基于一项开放标签、多中心的III期研究(XTEND-1)数据。该研究纳入了159例12岁及以上患者,旨在评估每周1次接受efanesoctocog alfa对既往接受过凝血因子VIII(FVIII)替代疗法的严重A型血友病患者的安全性、有效性和药代动力学特征。
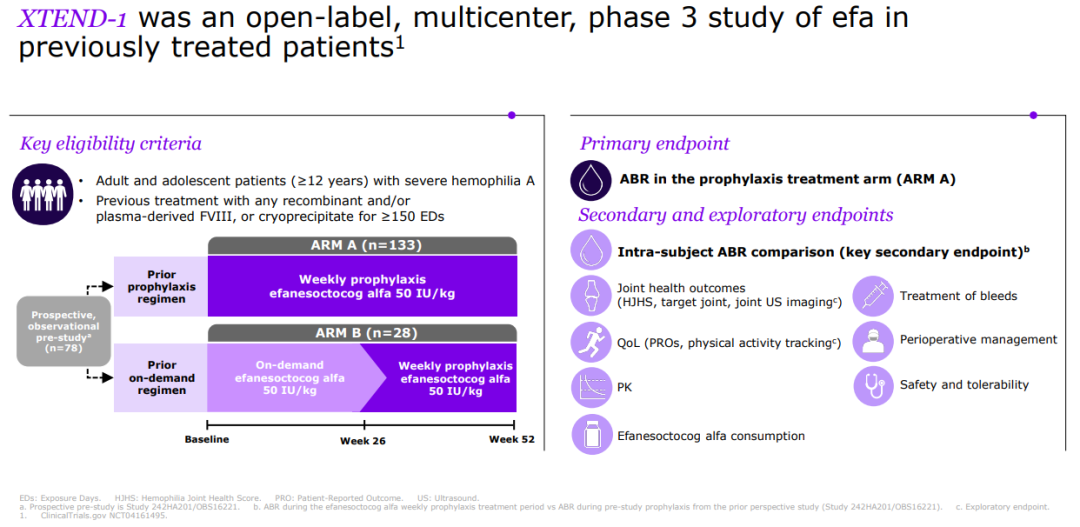
XTEND-1设计方案
XTEND-1设有两个平行组:A组即预防组(n=133)的成员每周给予50 IU/kg Efanesoctocog alfa,持续 52 周;B组即按需组(n=26)的成员最初根据需要给予50 IU/kg,持续 26 周,之后变成每周一次给药,持续 26 周。
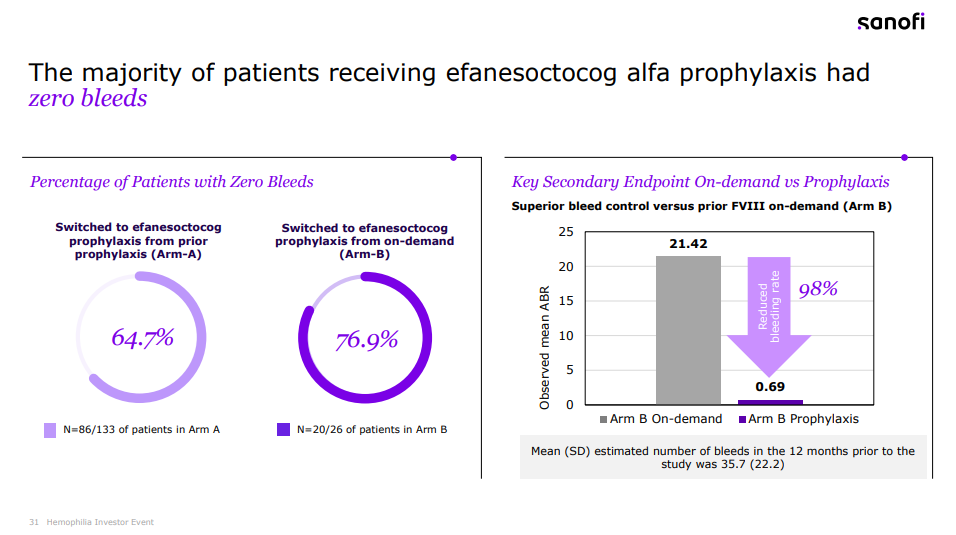
该研究的主要终点是A组的年出血率(ABR)。结果显示,在每周接受一次efanesoctocog alfa预防性治疗的A组患者中,52周内中位年出血率(ABR)为0,平均ABR为0.70,达到了具有临床意义的出血预防的主要终点。
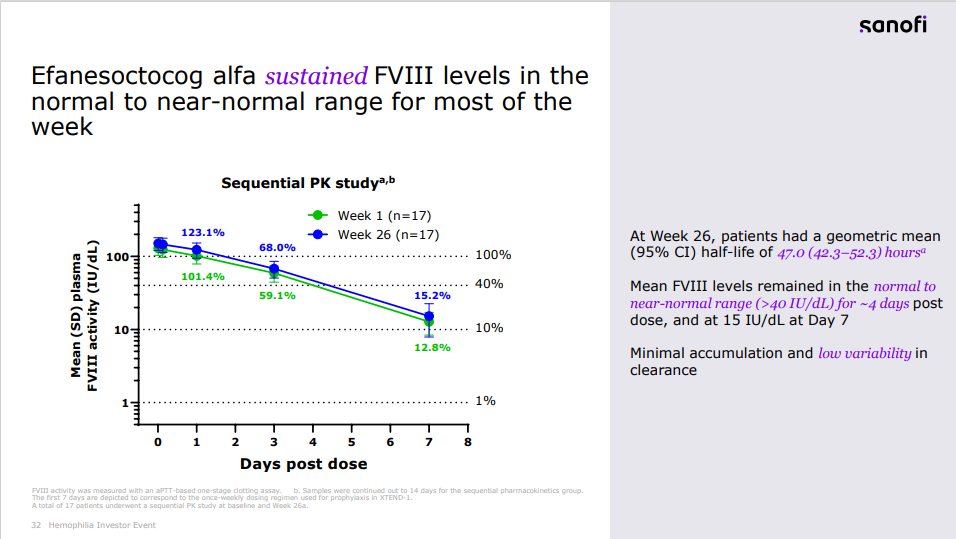
相较于先前预防性FVIII替代治疗,efanesoctocog alfa在预防出血事件方面表现出优效性。在一周的大部分时间里,efanesoctocog alfa可以维持FVIII水平在正常至接近正常范围内。
此外,XTEND-Kids的中期数据显示,12岁以下的儿童每周接受一次efanesoctocog alfa,持续26周(n=23),平均ABR为0.5,中位ABR为0。
赛诺菲首席执行官Paul Hudson表示:“今天Efanesoctocog alfa的获批使患者和医生能够重新定义血友病患者的生活。通过每周一次的剂量,Efanesoctocog alfa可持续性实现的凝血因子活性水平,有望改变血友病患者的出血状况。”

本文地址:http://www.cnzhilian.com/jiankang/2023-02-24/628879.html
友情提示:文章内容为作者个人观点,不代表本站立场且不构成任何建议,本站拥有对此声明的最终解释权。如果读者发现稿件侵权、失实、错误等问题,可联系我们处理
- 内蒙古煤矿坍塌事故调整救援方案 避免发生次生灾害影响2023-02-24 18:00:20
- 中央气象台:弱冷空气将影响华北东北2023-02-24 18:00:20
- 文化和旅游部:深化高校共建助推文化和旅游高质量发展2023-02-24 18:00:20
- 本轮疫情是否已经结束?官方最新研判2023-02-24 18:00:20
- 港深联合发布十六条措施促进跨境知识产权合作2023-02-24 18:00:20
-

 70岁以上老人核酸检测费用多少 新规定明天起不做核酸了吗
70岁以上老人核酸检测费用多少 新规定明天起不做核酸了吗
2022-11-07
-

 梅婷现任70岁老公曾剑个人资料(曾剑个人资料)
梅婷现任70岁老公曾剑个人资料(曾剑个人资料)
2022-09-08
-
烟台今天已封闭的小区 烟台现在封闭小区名单有哪些
2022-10-12 09:07:30
-
张家界桑植新娘吴梅婚纱照事件完整版 看女主出轨聊天内容视频
2022-11-11 14:27:00
-
目前南岸区及江北封闭小区名单有哪些 看最新封控通告
2022-11-11 14:49:26
-
无人售货机功能(无人自动售货机操作方法介绍)
2022-07-27 08:41:09
-
2022南宁封控小区名单表 南宁最新封闭小区名单2022年8月什么情况
2022-08-26 09:52:30