EMBO J:范祖森团队等揭示circRNA负向调控肠道干细胞自我更新的新机制
- 2023-02-09 18:00:22 健康一线
- 健康
肠道是体内最大的消化吸收器官和外周免疫器官,主要包括肠上皮和固有层两部分。肠上皮的所有成熟细胞均由位于隐窝底部的肠道干细胞产生,这些干细胞具有自我更新和分化能力。肠道干细胞作为肠道上皮的种子细胞,对于整个肠道上皮的更新和稳态维持至关重要。
范祖森课题组最近鉴定发现肠道上皮细胞新亚群Tuft2细胞具有抵抗病原体感染的作用,参与肠道黏膜稳态的维持(Immunity, 2022)。前期发现了长链非编码RNA lncGata6 调控肠道干细胞的自我更新(Nature Cell Biology, 2018)。发现肠道驻留ILC2 细胞分泌IL-13介导肠道干细胞高表达circPan3促进其再生能力(Nature Immunity, 2019)。还发现肠道神经细胞分泌的5-HT激活PGD2+巨噬细胞,使其产生PGE2继而激活Wnt信号通路促进肠道干细胞的干性(Cell Research, 2022)。并发现肠道神经细胞分泌的5-HT还能够激活肠癌干细胞的干性和肠癌发生,阻断5-HT信号显著抑制肠癌的发生和转移(Neuron, 2022)。
近日,中国科学院生物物理研究所范祖森课题组在 The EMBO Journal 期刊发表了题为:Noncoding RNA circBtnl1 suppresses self-renewal of intestinal stem cells via disruption of Atf4 mRNA stability 的研究论文。
该研究揭示了在肠道干细胞高表达的环状RNA-circBtnl1在稳态情况下抑制肠道干细胞的自我更新,并通过调控Atf4/Sox9信号调节干性维持的分子机制。
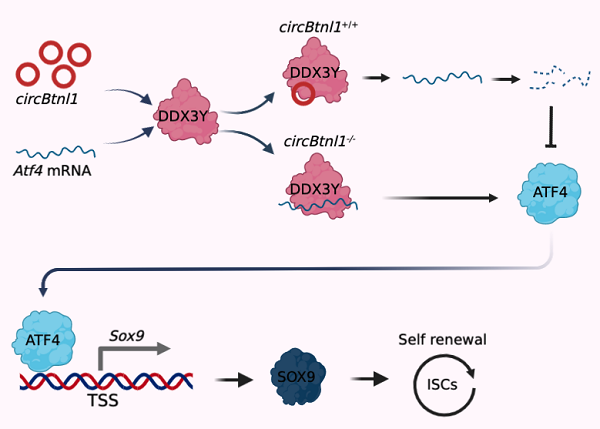
在该研究中,研究团队发现circBtnl1敲低能够促进肠道干细胞的增殖和类器官的生长。我们构建了circBtnl1敲除小鼠,发现circBtnl1缺失后小鼠肠道隐窝和肠绒毛明显增多,肠道干细胞的数目也显著增多。同时,circBtnl1敲除后并不影响其母基因Btnl1的mRNA和蛋白水平的表达,表明circBtnl1通过一种不依赖于Btnl1 mRNA和蛋白的方式调节肠道干细胞的自我更新能力。在稳态情况下,circBtnl1和RNA解旋酶Ddx3y竞争性结合转录因子Atf4的mRNA,进而抑制Atf4 mRNA的稳定性,继而抑制干性因子Sox9的转录表达,抑制肠道干细胞的再生能力,首次揭示circBtnl1对肠道稳态的负性调节作用。
总之,该研究揭示了非编码RNA circBtnl1负向调控肠道干细胞自我更新的新机制,发现了Atf4/Sox9信号参与干性稳态维持的新功能,为解析肠道干细胞的稳态调控机制提供了新视角。
circBtnl1负向调控肠道干细胞自我更新的分子机制
中国科学院生物物理研究所范祖森研究员、田勇研究员和郑州大学朱平平研究员为论文共同通讯作者,中国科学院生物物理研究所助理研究员郭晖和博士研究生张嘉航为并列第一作者。该研究得到了科技部重点研发计划、国家自然科学基金和中科院先导专项等经费支持。

本文地址:http://www.cnzhilian.com/jiankang/2023-02-09/627313.html
友情提示:文章内容为作者个人观点,不代表本站立场且不构成任何建议,本站拥有对此声明的最终解释权。如果读者发现稿件侵权、失实、错误等问题,可联系我们处理
- 幽门螺杆菌生物蛋白芯片分型检测:精准识别毒株,减少抗生素滥用2023-02-09 18:00:25
- 波士顿大学研究,每天一个鸡蛋,降低高血压、糖尿病风险2023-02-09 18:00:25
- Nutrients:每天2-3杯咖啡,血压更低2023-02-09 18:00:25
- Advanced Science:南大/药大团队首次证实,基于红细胞的新型液体活检可用于早期肺癌筛查和诊断2023-02-09 18:00:25
- 《科学》子刊:ALS患者的“智慧外骨骼”!哈佛科学家开发轻便可穿戴设备,协助ALS患者恢复上肢功能,穿戴负担单侧仅150g2023-02-09 18:00:25
-

 70岁以上老人核酸检测费用多少 新规定明天起不做核酸了吗
70岁以上老人核酸检测费用多少 新规定明天起不做核酸了吗
2022-11-07
-

 梅婷现任70岁老公曾剑个人资料(曾剑个人资料)
梅婷现任70岁老公曾剑个人资料(曾剑个人资料)
2022-09-08
-
烟台今天已封闭的小区 烟台现在封闭小区名单有哪些
2022-10-12 09:07:30
-
张家界桑植新娘吴梅婚纱照事件完整版 看女主出轨聊天内容视频
2022-11-11 14:27:00
-
目前南岸区及江北封闭小区名单有哪些 看最新封控通告
2022-11-11 14:49:26
-
无人售货机功能(无人自动售货机操作方法介绍)
2022-07-27 08:41:09
-
2022南宁封控小区名单表 南宁最新封闭小区名单2022年8月什么情况
2022-08-26 09:52:30
文章排行榜
- 周排名
- 月排名