2021年美国FDA批准50款新药上市
- 2022-01-24 09:20:23
- 药品
 |
|
|
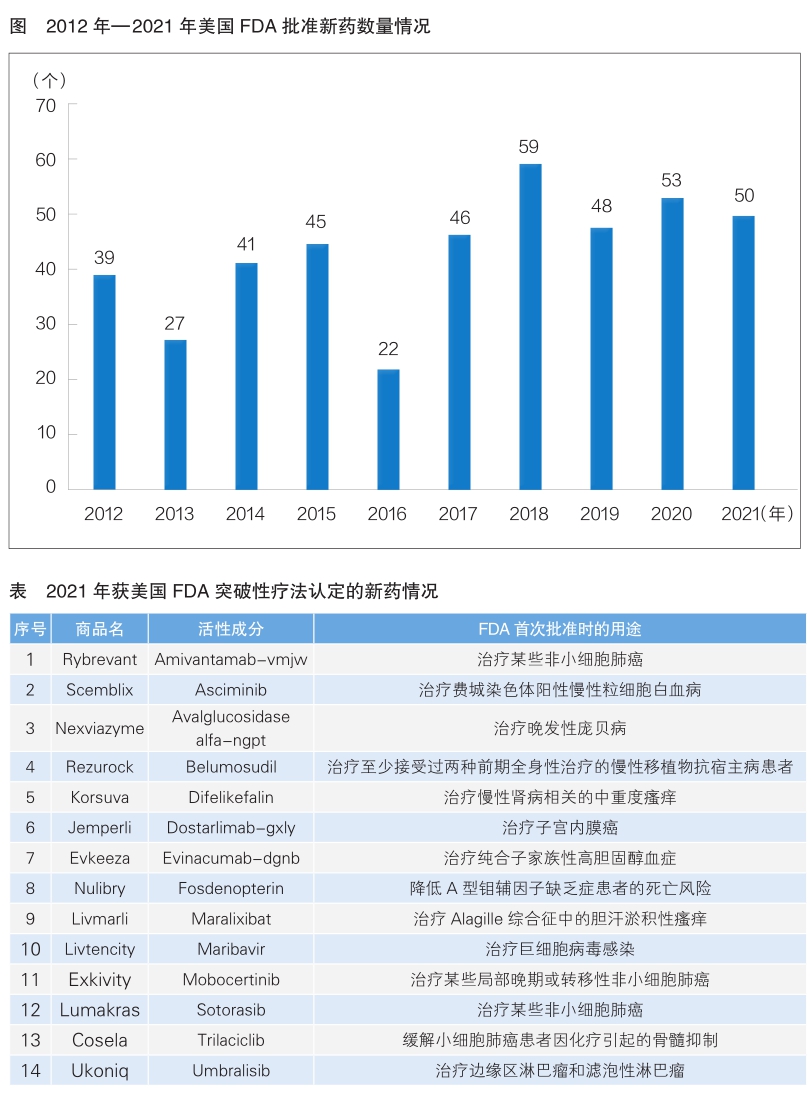
近日,美国食品药品管理局(FDA)药物评价和研究中心(CDER)发布2021年度新药获批报告。报告显示,2021年美国FDA共批准50款新药上市,在近十年每年获批新药数目中,该数字位列第三(详见图)。
从创新性上看,2021年美国FDA批准上市的新药中,有27款为first-in-class疗法,占全年获批新药总数的54%;从历史上看,无论是first-in-class新药的绝对数还是占比,都为近10年来的最高值。同时,这些新药的作用机制不同于已有疗法,有望为患者带来更多选择,为大众健康带来重要的积极影响。
另外,在上述50款新药中,有14款曾被美国FDA授予突破性疗法认定(详见表),该绝对数为2015年至今的第三名。与已有疗法相比,这些突破性疗法在治疗特定的严重疾病时,可能表现出更好的临床效益。
以下挑选一些完成“从0到1”突破的新药作简单介绍。
Lumakras:击破KRAS“不可成药”性
KRAS基因突变是癌症中最常见的突变之一,是业界著名的“不可成药”靶点。在非小细胞肺癌患者中,约有25%的患者会出现KRAS基因突变,其中13%为KRAS G12C突变。
Lumakr as是特异性靶向KRAS G12C突变体的共价抑制剂,它通过与KRAS G12C突变体结合,将KRAS锁死在失活状态,从而不可逆地抑制KRAS的活性。美国FDA肿瘤卓越中心主任、药物评估和研究中心肿瘤疾病办公室代理主任Richard Pazdur博士曾指出,KRAS突变一直难以被药物靶向,是未被满足的临床需求。此次Lumakras的获批,代表着个体化疗法的又一重大进步。
据了解,安进公司和百济神州已经达成合作,将共同进行Lumakras在中国的开发工作。
Cabenuva:首款长效HIV注射疗法
治疗HIV感染的鸡尾酒疗法是医学领域在过去25年中取得的最重要进展之一。只要患者坚持每日服药,他们的寿命就能与健康人没有显著区别。但是,每日服药对于很多患者来说是一个负担。
Cabenuva是FDA批准的首个用于HIV感染成人患者的完整注射方案,每月只需进行一次治疗,能够极大缓解患者每日服药的压力。Cabenuva是一款肌肉注射的长效抗病毒疗法,由利匹韦林和卡博特韦组成。利匹韦林是一款口服非核苷逆转录酶抑制剂;卡博特韦是一款整合酶抑制剂,它的作用是抑制病毒DNA整合到人体免疫细胞的基因组中。
Tezspire:造福严重哮喘患者
哮喘是一种高度异质性的疾病,影响着全球约3.4亿人的健康。另外,在哮喘患者中,约有10%属于严重哮喘。尽管他们可以使用吸入性的哮喘药物等疗法进行治疗,但许多严重哮喘患者的病情还是没有得到控制。而且因为严重哮喘本身的复杂性,许多患者具体的发病原因不明。
Tezspire是一款靶向抗胸腺基质淋巴细胞生成素(TSLP)的单克隆抗体疗法。TSLP是一种上皮细胞因子,位于多个炎症级联反应的顶端,能够启动过敏性、嗜酸性粒细胞和其他类型与严重哮喘相关的气道炎症的过度免疫反应。
该新药临床试验的主要研究者表示,很多严重哮喘患者仍然会频繁出现病情加重、生活质量严重降低、住院风险提高等情况。Tezspire为无法控制症状的严重哮喘患者提供了一种急需的新治疗选择。
Aduhelm:近20年来FDA批准的首款阿尔茨海默病新疗法
从提交申请到获批的半年后,行业里关于Aduhelm(Aducanumab)的讨论一直没有停止。从积极的角度看,人们期望它的获批能激发行业对阿尔茨海默病创新疗法的投入,进而鼓励更多创新疗法的到来。
阿尔茨海默病药物发现基金会(ADDF)创始执行董事兼首席科学官Howard Fillit博士认为,Aducanumab只是未来5~10年里有望造福患者的多个阿尔茨海默病新药中的一个。阿尔茨海默病领域丰富的研发管线以及更多生物标志物和其他重要研究工具的出现,意味着该领域目前正在进行的临床试验更为严格,新药的诞生也更具希望。
Welireg:诺奖信号通路研究催生的创新抗癌疗法
Von Hippel-Lindau综合征是一种罕见遗传疾病,它可异常激活癌症患者体内的缺氧诱导因子(HIF-2α)。HIF-2α在患者体内的积聚能导致良性和恶性肿瘤的形成,比如肾细胞癌、中枢神经系统血管母细胞瘤、胰腺神经内分泌肿瘤。
HIF-2α通路相关研究曾在2019年荣获诺贝尔生理学或医学奖。而Wel ireg作为一种强效、选择性新型口服HIF-2α抑制剂,是由该项研究成果转化而成的创新疗法。
Rybrevant:首款靶向不同肿瘤抗原的双特异性抗体
Rybrevant是一款人源化EGFR/MET双特异性抗体,是FDA批准的首款靶向不同肿瘤抗原的双特异性抗体疗法。它具有多重抗癌的作用机制,不但能够阻断EGFR和MET介导的信号传导,还可以引导免疫细胞靶向携带激活性和抗性EGFR/MET突变和扩增的肿瘤。
该疗法已被国家药监局纳入突破性治疗药物品种,目前在我国展开了多项临床试验。
Zynlonta:首款靶向CD19的抗体偶联药物
Zynlonta是首款获得FDA批准的靶向CD19的抗体偶联药物。该品将人源化的抗CD19单克隆抗体与名为吡咯并苯并二氮杂(PBD)二聚体的独特细胞毒素偶联在一起。CD19是B细胞表面表达的特异性抗原,是多种CAR-T疗法的靶点。PBD进入细胞之后,通过与DNA进行不可逆的结合,让DNA双螺旋的两条链之间产生交联,进而阻止DNA链的分离,最终导致癌细胞的死亡。
在我国,Zynlonta正由ADC Therapeutics与瓴路药业成立的合资公司Overland ADCT BioPharma开发。
Pepaxto:首个获批的肽偶联抗癌药物
Pepaxto是一款first-in-class肽偶联药物,它将烷化剂与靶向氨肽酶的多肽偶联在一起。Pepaxto由于其亲脂性能够迅速被多发性骨髓瘤细胞摄入,在细胞内,它会迅速被肽酶水解,从而释放具有亲水性的烷化剂。在体外实验中,Pepaxto由于能够提高烷化剂在细胞内的浓度,杀伤多发性骨髓瘤细胞的能力比其携带的烷化剂高50倍。
多肽类药物的分子量介于小分子药物和生物制品之间,与生物制品相比,多肽具有多种优点:设计更简单,能与未充分探索的靶标相互作用,具有更低的免疫原性和更好的组织渗透性。除了具有生物活性外,肽还能很好地将药物运送到特定的靶标。
Leqvio:首个降低“坏胆固醇”的siRNA疗法
Leqvio是一款first-in-class的siRNA疗法,可与编码PCSK9蛋白的mRNA结合,通过RNA干扰作用降低其水平,防止肝脏生产PCSK9蛋白。降低PCSK9蛋白水平后,更多低密度脂蛋白受体能回到肝细胞表面,清除血液中的低密度脂蛋白。这款疗法在初始注射和第三个月完成第二次注射治疗后,每年仅需两次治疗即可取得长效控制。未来,长效治疗是RNA干扰疗法的一个发展方向。
Verquvo:造福心衰患者
Verquvo是FDA在2021年批准的首款创新药,也是首个治疗慢性心力衰竭恶化患者的可溶性鸟苷酸环化酶(sGC)激动剂。
sGC对血管和心脏的功能都很重要,然而在心力衰竭患者体内,sGC不能被充分激活,从而导致心肌和血管功能异常。Verquvo能够通过激活sGC,恢复关键信号途径(NO-sGCcGMP)的功能。
(数据来源:FDA网站;药明康德内容团队供稿)
本文地址:http://www.cnzhilian.com/hangye/yaopin/2022-01-24/568449.html
友情提示:文章内容为作者个人观点,不代表本站立场且不构成任何建议,本站拥有对此声明的最终解释权。如果读者发现稿件侵权、失实、错误等问题,可联系我们处理
- 上一篇:手性纳米佐剂介导免疫应答 为疫苗研发提供理论支撑
- 下一篇:返回列表
- 2021年美国FDA批准50款新药上市2022-01-24 09:20:23
- “改革之手”点燃创新引擎 ——2021年获批上市创新药盘点2022-01-24 09:18:29
- 全国两会代表委员行业协会负责人为药监工作建言献策2022-01-24 09:18:04
- 在新的赶考路上踔厉奋发笃行不怠2022-01-24 09:17:46
- 清炖羊排,年夜饭必备菜,汤鲜味美软烂又不膻,吃肉又喝汤太赞了2022-01-24 08:00:09
-

 什么是阴痛?
什么是阴痛?
2021-10-26
-

 美立方国内外专家齐聚 颌面专家团再升级
美立方国内外专家齐聚 颌面专家团再升级
2021-08-23
-
《热点聚焦》医疗机构内新冠病毒感染防控有了新要求
2021-09-15 20:00:10
-
浙大一院2021年中秋节、国庆节放假及工作安排
2021-09-12 14:00:03
-
什么是阴结?
2021-10-26 10:33:42
-
名医风采 美立方颌面国际专家团,轮廓改造天团
2021-08-23 11:48:32
-
12333异地就医备案 您关心的都在这里
2021-09-07 10:40:49


